索菲恩生物科技(上海)有限公司
2 年
手机商铺
- NaN
- 0
- 0
- 1
- 0
推荐产品
公司新闻/正文
解码细胞器离子通道:细胞信号与稳态的守门人
5086 人阅读发布时间:2025-07-23 16:04
在细胞的复杂网络中,离子通道不仅存在于质膜,同样也广泛分布于细胞内部的各类细胞器:如溶酶体、线粒体、内质网和细胞核。它们是维持细胞功能和应答外界刺激的关键“通道”,也是许多疾病发生的关键节点。
为什么研究细胞器离子通道如此重要?
◆ 它们调控离子梯度与跨膜电位
◆ 涉及钙信号传导、pH调节、细胞凋亡等核心机制
◆ 与众多重大疾病密切相关,如:神经退行性疾病,癌症,代谢综合征,溶酶体贮积病。
不同细胞器中的离子通道作用概览
溶酶体
◆ 维持酸性环境以降解生物大分子
◆ 通道功能异常可阻碍自噬,引发神经退行性变化
线粒体
◆ 离子通道参与能量代谢与凋亡调控
◆ 功能失衡会导致氧化磷酸化障碍与异常细胞死亡
内质网
◆ 储存和释放钙离子
◆ 参与肌肉收缩、分泌、增殖等
◆ 通道失调与代谢病和应激损伤密切相关
细胞核
◆ 尽管研究较少,但越来越多证据表明它们参与基因表达与染色质重塑
细胞器离子通道在细胞生命活动中承担着核心调控功能,其作用远非边缘化。深入解析这些通道的生理与病理机制,将为靶向性药物的设计与开发提供新的理论依据和方向。
Qube 384全自动膜片钳系统推动离子通道研究进入“细胞器时代”
使用Qube 384自动化膜片钳系统建立STIM1/Orai1钙电流记录平台
STIM1/Orai1介导的钙电流ICRAC是细胞钙信号研究中的重要方向,亦是多种生理及病理状态(如免疫应答、肿瘤进展)中的关键调控环节。通过Sophion Bioscience的Qube 384系统建立的全自动化膜片钳测定方法,用于高通量、标准化地记录STIM1/Orai1通道活性,为钙信号机制研究与药物筛选提供了有效技术平台。
钙离子(Ca²⁺)是细胞信号传导的核心第二信使,广泛参与胞内外稳态维持、细胞增殖、分化等过程。在内质网钙储耗竭后,STIM1/Orai1复合体形成ICRAC通道,引发储存操作性钙进入(Store-operated calcium entry, SOCE)。该机制可通过膜片钳技术直接记录通道电流变化,但传统手工膜片钳耗时耗力,难以满足高通量筛选的需求。
使用Sophion Bioscience的Qube 384全自动化膜片钳平台建立STIM1/Orai1记录方法。该平台具有如下特点:
• 可同时进行384孔通道记录;
• 提供GΩ级封接质量;
• 支持完整协议设计与液体处理;
• 全自动化运行,适用于高通量化合物筛选。

采用两种不同策略激活ICRAC:
•细胞内液更换法 Exchange Intracellular Solution(IP₃激活):
通过Qube系统内液体通道交换引入IP₃,诱导ER钙储耗竭并激活STIM1/Orai1。使用期间需临时取出QChip进行处理,稍有时间滞后。
•细胞破膜释放预载激动剂法 Whole cell caging of Agonist:
在打破膜前向内液预加载IP₃,通过膜破裂后激活通道,避免激活延迟。提高了激活精度与实验效率。

通过添加钙通道阻断剂进行药理学验证,结果表明:
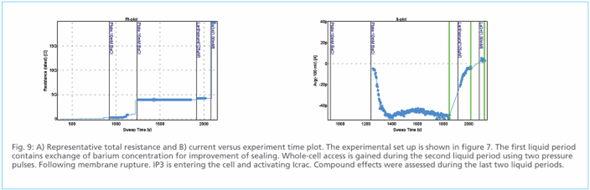
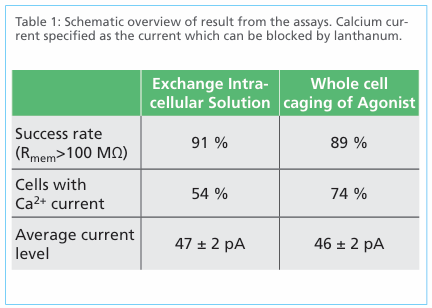
以上数据显示,Qube 384平台在两种激活策略下均能实现高重复性和有效记录。
该全自动化膜片钳方案不仅实现了STIM1/Orai1通道电流的高质量记录与验证,更显著简化了药物筛选流程,减少后续验证工作量。
细胞器离子通道不只是“背景角色”,它们是调节细胞命运的核心“枢纽”。理解其功能与病理机制,将为我们开发新型靶向药物提供崭新方向。未来,Qube 384有望成为钙信号研究与新药筛选的重要技术平台。